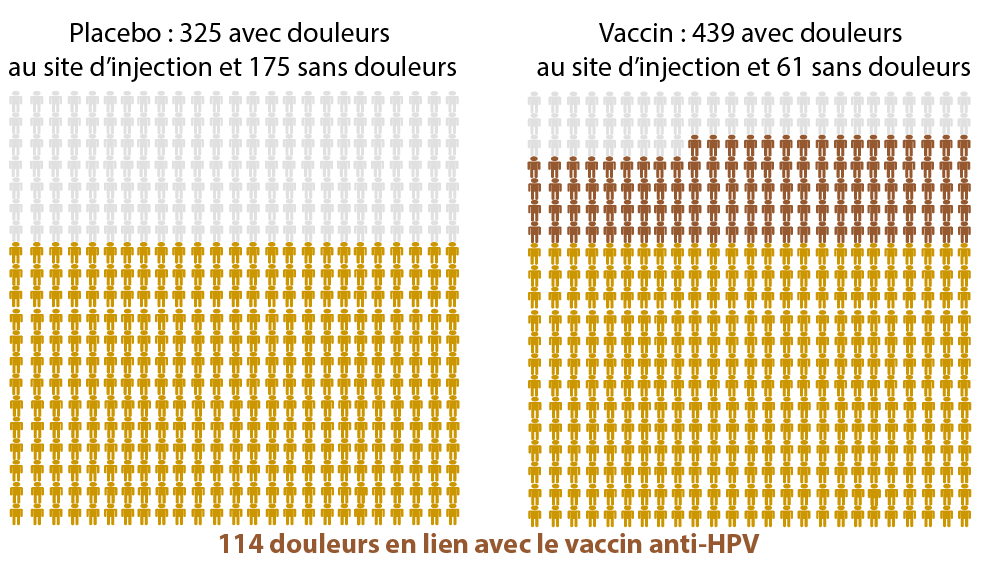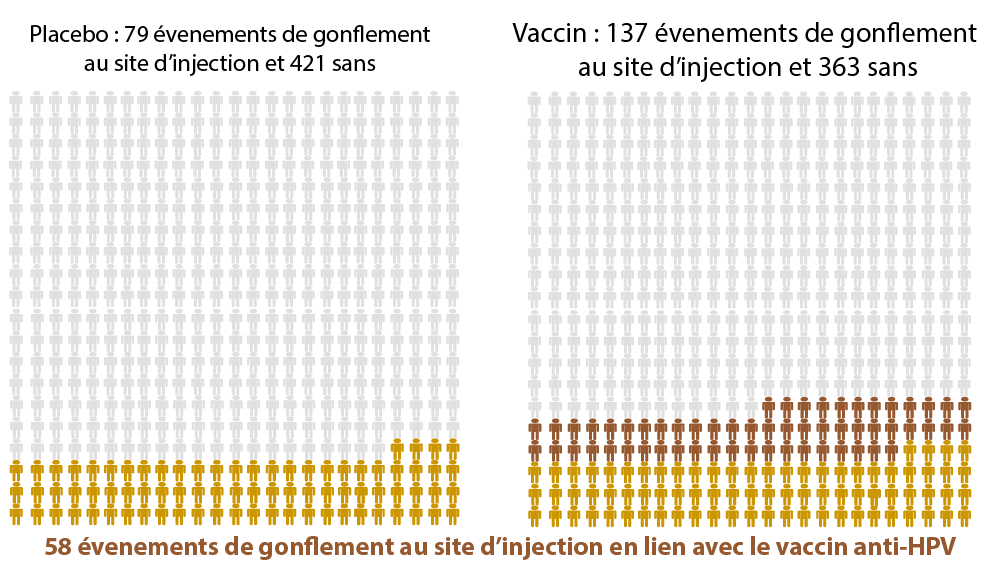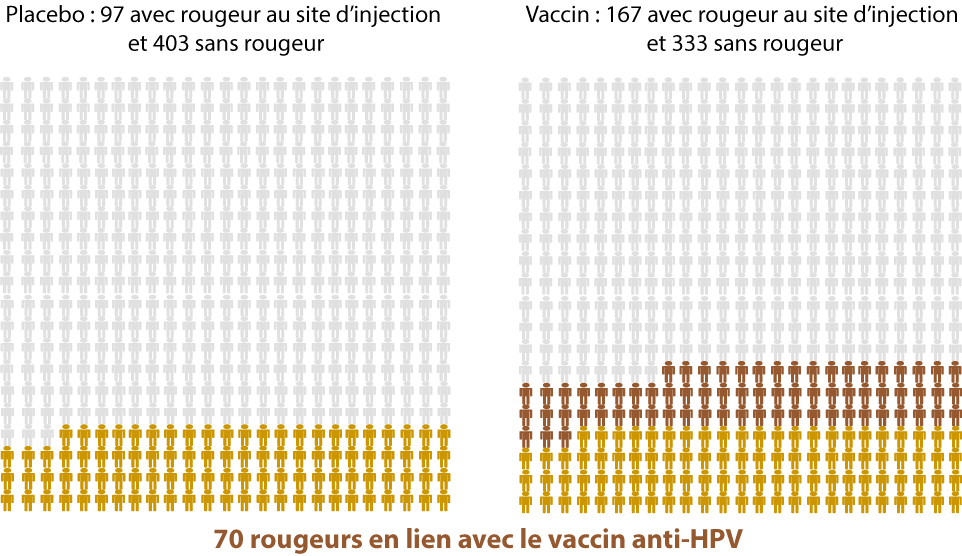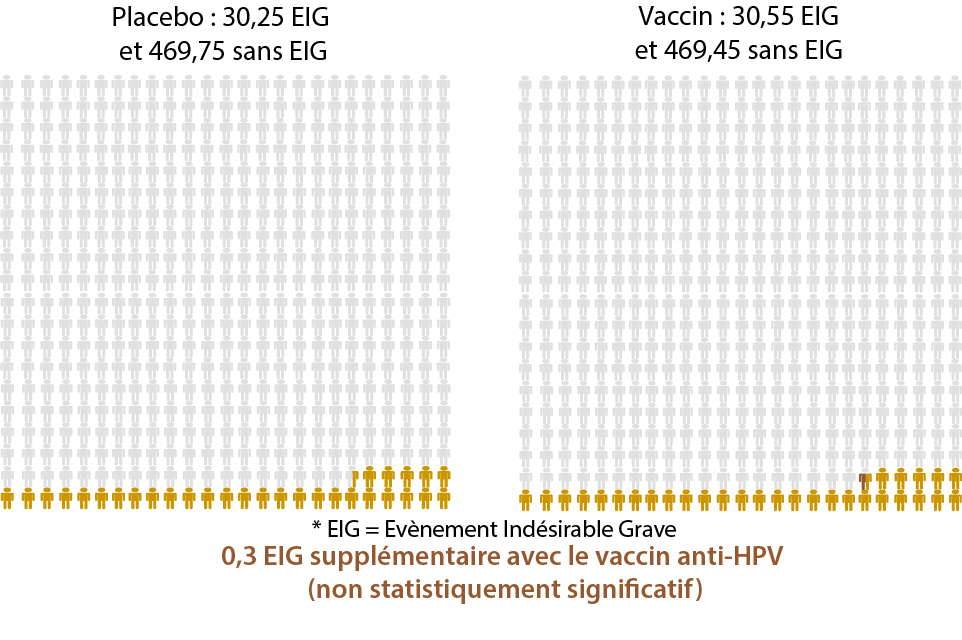Les Papillomavirus Humains (HPV), qu’est-ce que c'est?
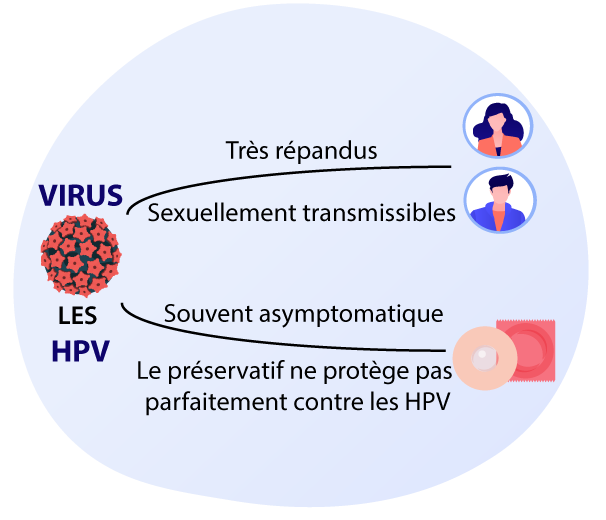
Les PapillomaVirus Humains (HPV) sont un groupe de virus très répandu. Il s’agit d’une infection sexuellement transmissible dont le port du préservatif ne protège que partiellement.
Aussi bien les hommes que les femmes peuvent être contaminés par le HPV.
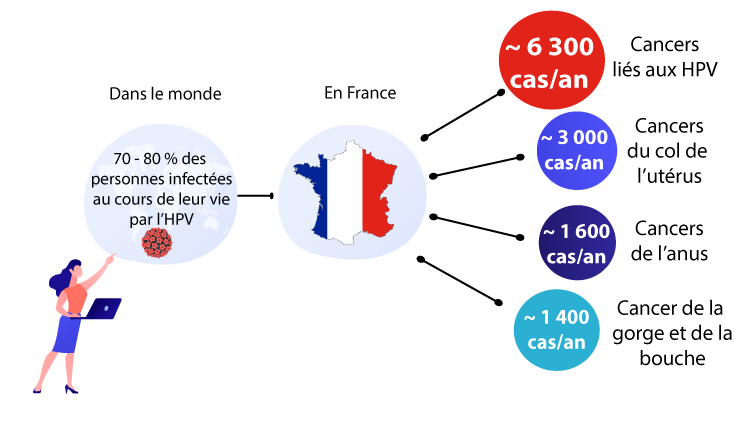
Quelques chiffres clés des infections à papillomavirus
On estime que 70% à 80% des personnes sexuellement actives seront infectées au moins une fois dans leur vie par un HPV. Selon l’Institut National du Cancer, plus de 6 300 cancers par an étaient liés aux HPV en 2015.
Le cancer le plus fréquent lié aux HPV est le cancer du col de l’utérus. En France, il y a près de 3000 nouveaux cas par an du cancer du col de l’utérus et 1 100 décès par an sont dus à ce cancer. Un autre cancer fréquent lié aux HPV est le cancer de l’anus (environ 1600 cas chaque année) (1).
Les maladies liées aux HPV
Il existe environ 200 types différents de ce virus. La plupart du temps, l’organisme humain élimine spontanément le virus, mais dans près de 10 % des cas, l’infection persiste et peut entraîner plusieurs années plus tard des lésions précancéreuses qui peuvent évoluer ensuite vers un cancer.
Une douzaine de types sont des virus « à haut risque » oncogène c’est-à-dire pouvant être responsables de cancers.
D’autres souches peuvent donner des lésions bénignes de type verrues génitales appelées condylomes. La plupart du temps, l’organisme humain élimine spontanément le virus, mais dans près de 10% des cas, l’infection persiste et peut entraîner plusieurs années plus tard des lésions précancéreuses qui peuvent évoluer ensuite vers un cancer (1).
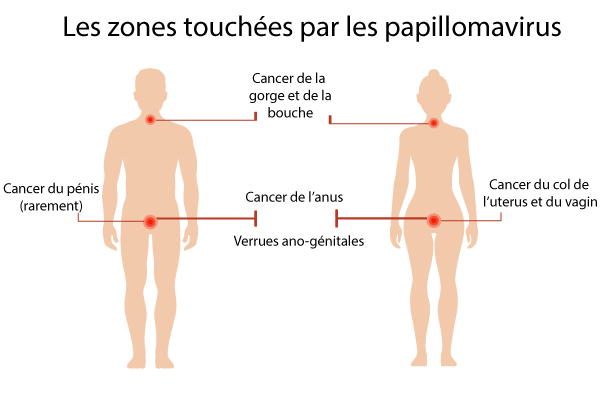
Quelles sont les zones touchées et les cancers liés aux papillomavirus humains?
Il existe plusieurs types de cancers liés aux HPV :
- cancer du col de l’utérus
- cancer de la vulve
- cancer de l’anus
- cancer de la bouche et de la gorge
- cancer du pénis (plus rarement) (2)
Prenons l'exemple du col de l'utérus
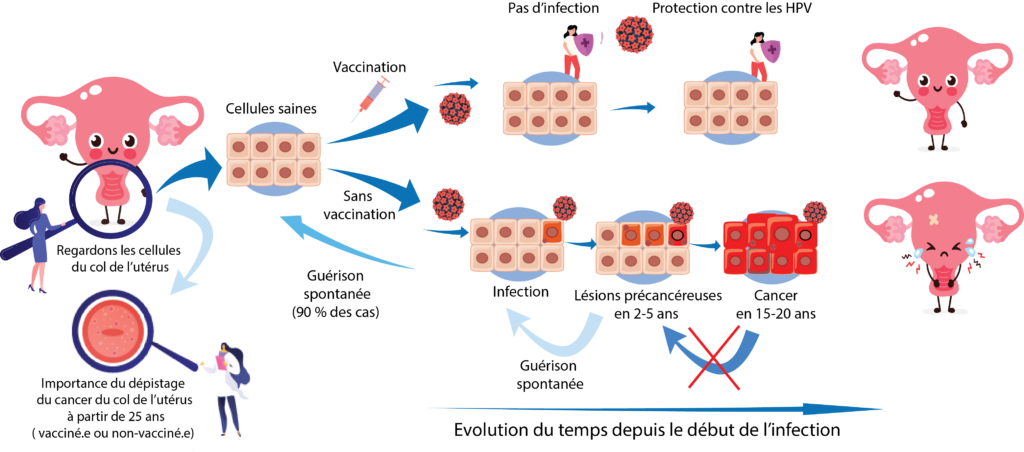
Vaccination et infections HPV
-
La vaccination contre les papillomavirus humains prévient les infections par les souches de HPV concernées par le vaccin. Le vaccin est plus efficace lorsque celui-ci est réalisé avant l’exposition au virus.
-
90% des cas de cancers induits par les HPV sont dus à des types ciblés par le vaccin nonavalent (HPV 6, 11, 16, 18, 31, 33, 45, 52, 58) (3).
-
Le vaccin appelé GARDASIL® nonavalent est recommandé depuis 2018 faisant suite au GARDASIL® quadrivalent (6, 11, 16,18) recommandé depuis 2007.
-
En France, le vaccin est destiné pour toutes les jeunes filles et tous les jeunes garçons de 11 à 14 ans avec un rattrapage possible jusqu’à 19 ans.
-
Deux injections sont à réaliser entre 11 et 14 ans (à 0 puis 6 mois plus tard).
-
A partir de 15 ans, 3 injections seront à réaliser (à 0, 2 et 6 mois).

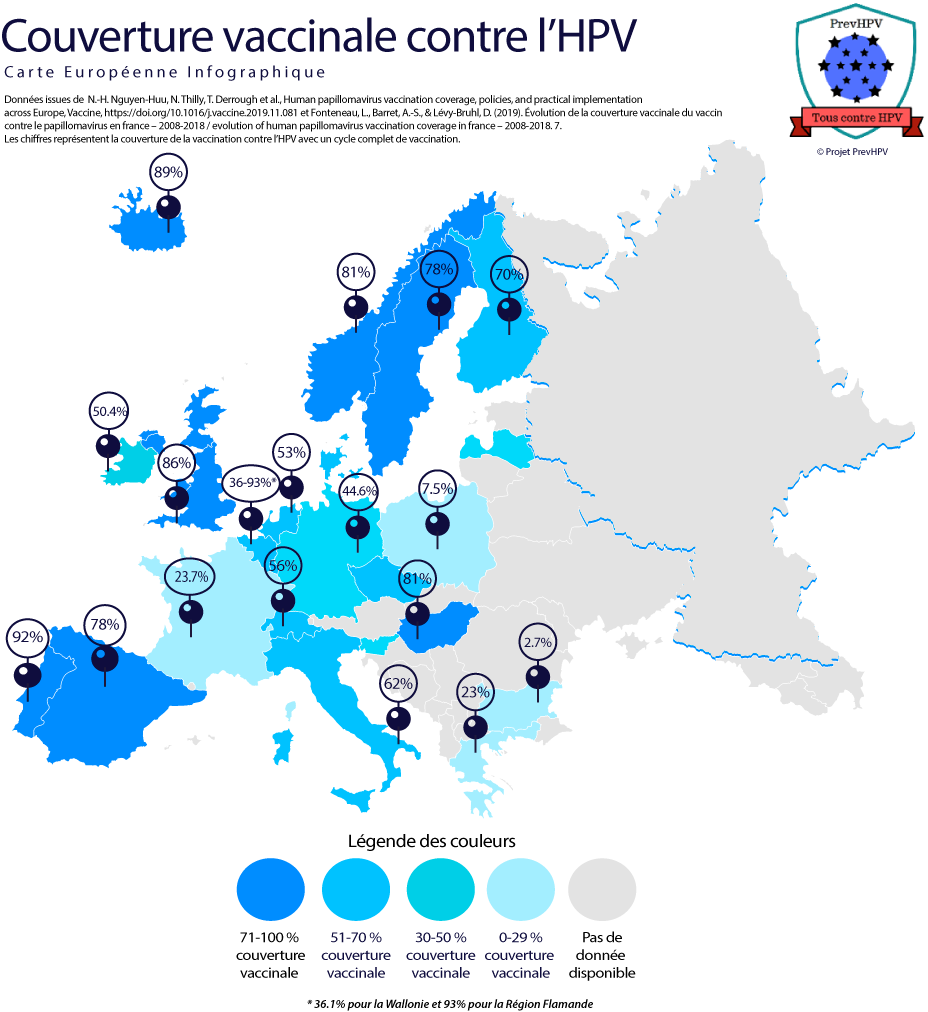
Couverture vaccinale en Europe (4,17)
L’efficacité du vaccin
Impact de la vaccination sur les lésions précancéreuses du col de l'utérus:
Il faut plusieurs dizaines d’années avant de constater une efficacité du vaccin sur l’apparition du cancer néanmoins des études ont déjà montré l’efficacité du vaccin sur les lésions précancéreuses de type CIN2+ (5)

8,5 lésions évitées grâce à la vaccination
Protection contre le cancer du col de l'utérus:
Une étude suédoise a suivi 1 672 983 femmes âgées de 10 à 30 ans de 2006 à 2017. Cette étude a montré une diminution du nombre de nouveaux cas de cancer du col de l’utérus chez les femmes vaccinées. Ce suivi est encore court pour l’apparition de cancer mais il s’agit de la première étude montrant un signal d’efficacité du vaccin sur le cancer du col utérin (6) . Une autre étude de cohorte danoise montre des chiffres similaires, avec une diminution de l’incidence cumulée de 11,3 / 100.000 chez les non vaccinées à 6,7 / 100.000 chez les vaccinées (vaccinées principalement entre 20 et 30 ans) (19).
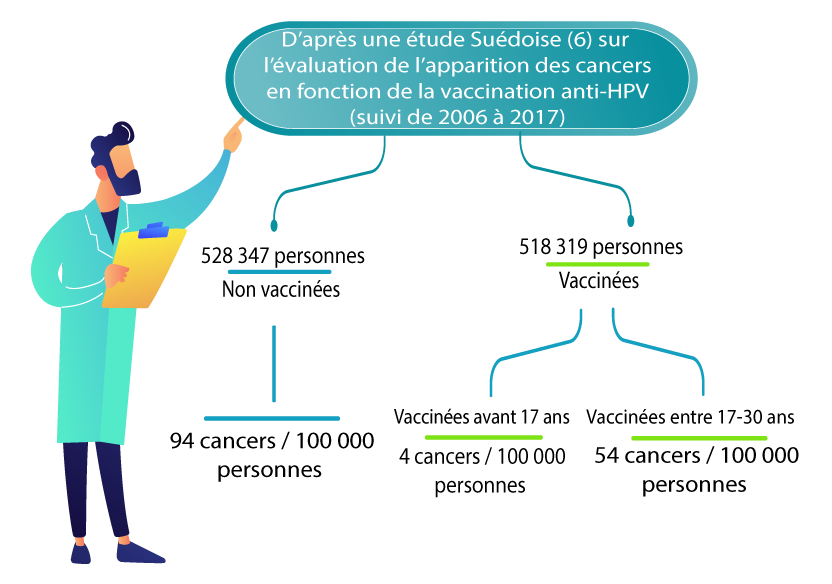
Des résultats similaires sont également retrouvés dans une étude de cohorte anglaise publiée en novembre 2021. Elle confirme une réduction de l’incidence du cancer du col de l’utérus, en particulier si la couverture vaccinale est élevée et si les femmes se voient proposer le vaccin à un plus jeune âge (20).
Protection contre les autres cancers HPV induits:
Des données commencent à être publiées concernant la diminution des cancers HPV induits chez les patients vaccinés contre le HPV.
Le registre des cancers finlandais a montré une protection sur tous les cancers HPV induits (notamment cancer de la vulve et cancer de la gorge et de la bouche). Il n’y avait pour l’instant que 7 ans de suivi. Il est encore trop tôt pour avoir des données chiffrées fiables mais ces données sont encourageantes (7)
Protection contre les condylomes / verrues génitales:

Les verrues anogénitales (ou condylomes) sont très fréquentes chez la femme comme chez l’homme (entre 94920 et 117888 nouveaux cas par an en France). Elles sont fortement contagieuses et touchent majoritairement les jeunes adultes. Elles sont systématiquement induites par des HPV. Les types 6 et 11 sont retrouvés dans 90% des cas de condylomes. En général, les lésions en elles-mêmes ne sont pas douloureuses, même si certains patients peuvent ressentir des démangeaisons, des sensations de brûlure ou d’irritation. Néanmoins, ces lésions inesthétiques sont récidivantes et leur prise en charge est particulièrement longue et douloureuse (8).
Après 5 à 8 ans de vaccination, en vie réelle, il a été noté une diminution de diagnostic de verrues anogénitales de 67% pour les femmes âgées de 15 à 19 ans et 48% pour les hommes. Dans les pays avec une couverture vaccinale supérieure à 50% ces chiffres passent à 88% chez les femmes et 86% chez les hommes (9).
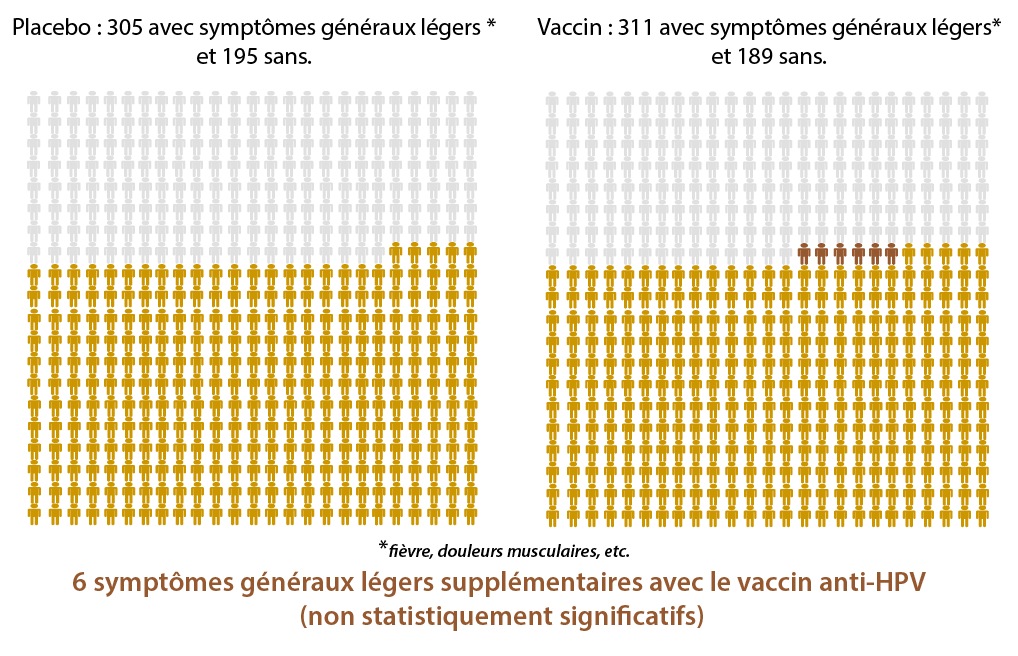
Les effets secondaires du vaccin (5)
Les différences statistiquement significatives entre un placebo et le vaccin anti-HPV
(= ces différences semblent être directement liées au vaccin anti-HPV)
Sur 500 personnes …
Les différences non statistiquement significatives entre un placebo et le vaccin anti-HPV
(= ces différences ne semblent pas être directement liées au vaccin anti-HPV)
Maladies auto-immunes
Syndrome de Guillain-Barré (SGB) est une affection rare dans laquelle le système immunitaire du patient attaque les nerfs périphériques. La plupart des personnes atteintes du syndrome de Guillain Barré se rétablissent pleinement, même dans les cas les plus graves. (10)
Concernant le lien entre la vaccination et le SGB les données sont discordantes.
Une étude de pharmaco-épidémiologie française a retrouvé un surrisque de SGB de l’ordre de 1 à 2 cas supplémentaire pour 100000 jeunes filles vaccinées. (11) Le lien entre SGB et vaccin HPV n’a pas été retrouvé dans plusieurs autres études (12,13,18).
Le comité consultatif mondial pour la sécurité des vaccins (GACVS) a considéré le vaccin comme « extrêmement sûr » dans son rapport de Juillet 2017. Il ne retient pas le SGB comme effet indésirable du vaccin. (15)
Allergies graves
Risque d’anaphylaxie (allergie grave) : environ 1,7 cas par million de doses (14)
Pensez à ce qui pourrait vous aider à prendre votre décision pour la vaccination anti HPV. Dans quelle mesure est-il important que vous :
Carte mentale
Le Papillomavirus Humain (HPV), qu’est-ce que?
Les chiffres clés
La couverture vaccinale
Les zones touchées